Depuis le début des temps, les êtres humains ont cherché à comprendre de quoi est composé l'univers et tout ce qu'il contient. Et tandis que les anciens mages et philosophes concevaient un monde composé de quatre ou cinq éléments - la terre, l'air, l'eau, le feu (et le métal, ou la conscience) - par l'Antiquité classique, les philosophes ont commencé à théoriser que toute la matière était en fait constituée de minuscules, atomes invisibles et indivisibles.
Depuis ce temps, les scientifiques se sont engagés dans un processus de découverte continue avec l'atome, espérant découvrir sa vraie nature et sa composition. Au 20e siècle, notre compréhension s'est affinée au point que nous avons pu en construire un modèle précis. Et au cours de la dernière décennie, notre compréhension a progressé encore plus, au point que nous en sommes venus à confirmer l'existence de presque toutes ses parties théorisées.
Aujourd'hui, la recherche atomique se concentre sur l'étude de la structure et de la fonction de la matière au niveau subatomique. Cela consiste non seulement à identifier toutes les particules subatomiques que l'on pense constituer un atome, mais à enquêter sur les forces qui les gouvernent. Il s'agit notamment de forces nucléaires fortes, de forces nucléaires faibles, de l'électromagnétisme et de la gravité. Voici une ventilation de tout ce que nous avons appris jusqu'à présent sur l'atome…
Structure de l'atome:
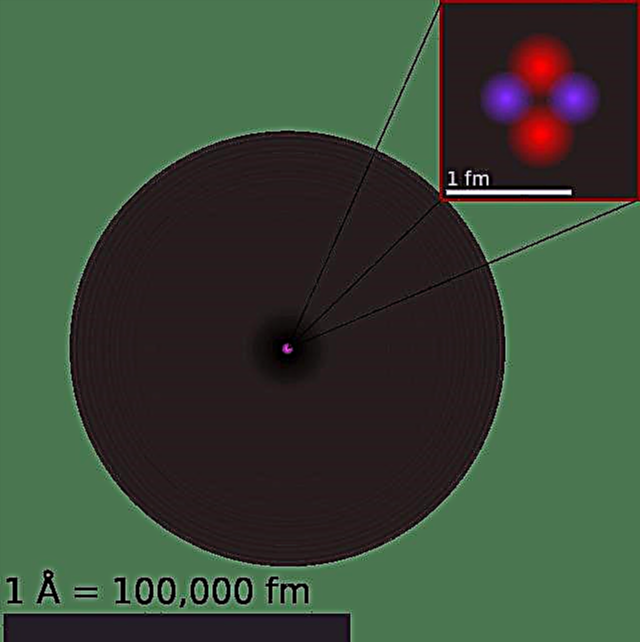
Notre modèle actuel de l'atome peut être décomposé en trois parties constituantes - les protons, les neutrons et les électrons. Chacune de ces parties a une charge associée, avec des protons portant une charge positive, des électrons ayant une charge négative et des neutrons sans charge nette. Conformément au modèle standard de la physique des particules, les protons et les neutrons constituent le noyau de l'atome, tandis que les électrons en orbite autour d'un «nuage».

Les électrons d'un atome sont attirés par les protons du noyau par la force électromagnétique. Les électrons peuvent s'échapper de leur orbite, mais uniquement en réponse à l'application d'une source d'énergie externe. Plus l'orbite de l'électron est proche du noyau, plus la force d'attraction est grande; par conséquent, plus la force externe nécessaire pour faire s'échapper un électron est forte.
Les électrons tournent autour du noyau sur plusieurs orbites, chacune correspondant à un niveau d'énergie particulier de l'électron. L'électron peut changer son état à un niveau d'énergie plus élevé en absorbant un photon avec suffisamment d'énergie pour le propulser dans le nouvel état quantique. De même, un électron dans un état d'énergie supérieur peut passer à un état d'énergie inférieur tout en rayonnant l'énergie excédentaire sous forme de photon.
Les atomes sont électriquement neutres s'ils ont un nombre égal de protons et d'électrons. Les atomes qui ont un déficit ou un surplus d'électrons sont appelés ions. Les électrons les plus éloignés du noyau peuvent être transférés vers d'autres atomes voisins ou partagés entre les atomes. Par ce mécanisme, les atomes peuvent se lier à des molécules et à d'autres types de composés chimiques.
Ces trois particules subatomiques sont des fermions, une classe de particules associées à de la matière de nature élémentaire (électrons) ou composite (protons et neutrons). Cela signifie que les électrons n'ont pas de structure interne connue, tandis que les protons et les neutrons sont constitués d'autres particules subatomiques. appelés quarks. Il existe deux types de quarks dans les atomes, qui ont une charge électrique fractionnée.

Les protons sont composés de deux quarks «up» (chacun avec une charge de +2/3) et d'un quark «down» (-1/3), tandis que les neutrons se composent d'un quark up et de deux quarks down. Cette distinction explique la différence de charge entre les deux particules, qui correspond à une charge de +1 et 0 respectivement, tandis que les électrons ont une charge de -1.
Les autres particules subatomiques comprennent les leptons, qui se combinent avec les fermions pour former les blocs de construction de la matière. Il existe six leptons dans le modèle atomique actuel: les particules d'électrons, de muons et de tau et leurs neutrinos associés. Les différentes variétés de particules de Lepton, communément appelées «saveurs», se différencient par leur taille et leurs charges, ce qui affecte le niveau de leurs interactions électromagnétiques.
Ensuite, il y a les bosons de jauge, qui sont connus comme des «porteurs de force» car ils assurent la médiation des forces physiques. Par exemple, les gluons sont responsables de la force nucléaire puissante qui maintient les quarks ensemble, tandis que les bosons W et Z (toujours hypothétiques) seraient responsables de la faible force nucléaire derrière l'électromagnétisme. Les photons sont la particule élémentaire qui compose la lumière, tandis que le boson de Higgs est chargé de donner aux bosons W et Z leur masse.
Masse atomique:
La majorité de la masse d’un atome provient des protons et des neutrons qui composent son noyau. Les électrons sont les particules les moins massives d'un atome, avec une masse de 9,11 x 10-31 kg et une taille trop petite pour être mesurée par les techniques actuelles. Les protons ont une masse qui est 1 836 fois celle de l'électron, à 1,6726 × 10-27 kg, tandis que les neutrons sont les plus massifs des trois, à 1,6929 × 10-27 kg (1 839 fois la masse de l'électron).

Le nombre total de protons et de neutrons dans le noyau d’un atome (appelés «nucléons») est appelé le nombre de masse. Par exemple, l'élément Carbon-12 est ainsi nommé parce qu'il a un nombre de masse de 12 - dérivé de ses 12 nucléons (six protons et six neutrons). Cependant, les éléments sont également organisés en fonction de leur numéro atomique, qui est le même que le nombre de protons trouvés dans le noyau. Dans ce cas, Carbon a un numéro atomique de 6.
La masse réelle d'un atome au repos est très difficile à mesurer, car même les atomes les plus massifs sont trop légers pour être exprimés en unités conventionnelles. En tant que tel, les scientifiques utilisent souvent l'unité de masse atomique unifiée (u) - également appelée dalton (Da) - qui est définie comme un douzième de la masse d'un atome neutre libre de carbone-12, qui est d'environ 1,66 × 10-27 kg.
Les chimistes utilisent également des moles, une unité définie comme une mole de tout élément ayant toujours le même nombre d'atomes (environ 6,022 × 1023). Ce nombre a été choisi de sorte que si un élément a une masse atomique de 1 u, une mole d'atomes de cet élément a une masse proche d'un gramme. En raison de la définition de l'unité de masse atomique unifiée, chaque atome de carbone 12 a une masse atomique d'exactement 12 u, et donc une mole d'atomes de carbone 12 pèse exactement 0,012 kg.
Désintégration radioactive:
Deux atomes qui ont le même nombre de protons appartiennent au même élément chimique. Mais les atomes avec un nombre égal de protons peuvent avoir un nombre différent de neutrons, qui sont définis comme étant des isotopes différents du même élément. Ces isotopes sont souvent instables, et tous ceux dont le numéro atomique est supérieur à 82 sont connus pour être radioactifs.
Lorsqu'un élément subit une décomposition, son noyau perd de l'énergie en émettant un rayonnement - qui peut être composé de particules alpha (atomes d'hélium), de particules bêta (positrons), de rayons gamma (énergie électromagnétique à haute fréquence) et d'électrons de conversion. Le taux auquel un élément instable se désintègre est connu comme sa «demi-vie», qui est le temps nécessaire à l'élément pour tomber à la moitié de sa valeur initiale.
La stabilité d'un isotope est affectée par le rapport protons / neutrons. Sur les 339 différents types d'éléments qui se produisent naturellement sur Terre, 254 (environ 75%) ont été étiquetés comme «isotopes stables» - c'est-à-dire non sujets à la décomposition. 34 éléments radioactifs supplémentaires ont des demi-vies supérieures à 80 millions d'années et existent également depuis le début du système solaire (d'où la raison pour laquelle ils sont appelés «éléments primordiaux»).
Enfin, 51 autres éléments à vie courte sont connus pour se produire naturellement, en tant qu '«éléments filles» (c.-à-d. Sous-produits nucléaires) de la désintégration d'autres éléments (comme le radium provenant de l'uranium). De plus, les éléments radioactifs à courte durée de vie peuvent être le résultat de processus énergétiques naturels sur Terre, tels que le bombardement de rayons cosmiques (par exemple, le carbone 14, qui se produit dans notre atmosphère).
Histoire de l'étude:
Les premiers exemples connus de la théorie atomique proviennent de la Grèce antique et de l'Inde, où des philosophes tels que Démocrite ont postulé que toute la matière était composée de minuscules unités indivisibles et indestructibles. Le terme «atome» a été inventé dans la Grèce antique et a donné naissance à l'école de la pensée connue sous le nom d '«atomisme». Cependant, cette théorie était plus un concept philosophique que scientifique.
Ce n'est qu'au XIXe siècle que la théorie des atomes s'est articulée comme une question scientifique, avec les premières expériences fondées sur des preuves. Par exemple, au début des années 1800, le scientifique anglais John Dalton a utilisé le concept de l'atome pour expliquer pourquoi les éléments chimiques réagissaient de certaines manières observables et prévisibles.
Dalton a commencé par se demander pourquoi les éléments réagissaient dans des rapports de petits nombres entiers, et a conclu que ces réactions se produisaient en multiples de nombres entiers d'unités discrètes - en d'autres termes, des atomes. À travers une série d'expériences impliquant des gaz, Dalton a développé ce qui est connu comme la théorie atomique de Dalton, qui reste l'une des pierres angulaires de la physique et de la chimie modernes.
La théorie se résume à cinq prémisses: les éléments, dans leur état le plus pur, sont constitués de particules appelées atomes; les atomes d'un élément spécifique sont tous les mêmes jusqu'au dernier atome; les atomes de différents éléments peuvent être différenciés par leur poids atomique; les atomes des éléments s'unissent pour former des composés chimiques; les atomes ne peuvent être ni créés ni détruits par réaction chimique, seul le groupement change jamais.
À la fin du 19e siècle, les scientifiques ont commencé à théoriser que l'atome était composé de plus d'une unité fondamentale. Cependant, la plupart des scientifiques se sont aventurés sur le fait que cette unité aurait la taille du plus petit atome connu - l'hydrogène. Et puis en 1897, à travers une série d'expériences utilisant des rayons cathodiques, le physicien J.J. Thompson a annoncé qu'il avait découvert une unité 1000 fois plus petite et 1800 fois plus légère qu'un atome d'hydrogène.

Ses expériences ont également montré qu'elles étaient identiques aux particules dégagées par l'effet photoélectrique et par les matières radioactives. Des expériences ultérieures ont révélé que cette particule transportait du courant électrique à travers des fils métalliques et des charges électriques négatives à l'intérieur des atomes. D'où la raison pour laquelle la particule - qui était à l'origine nommée «corpuscule» - a ensuite été changée en «électron», après la prédiction de la particule de George Johnstone Stoney en 1874.
Cependant, Thomson a également postulé que les électrons étaient distribués dans tout l'atome, qui était une mer uniforme de charge positive. Ceci est devenu connu sous le nom de «modèle de pudding aux prunes», qui se révélera plus tard faux. Cela a eu lieu en 1909, lorsque les physiciens Hans Gieger et Ernest Marsden (sous la direction d'Ernest Rutherfod) ont mené leur expérience en utilisant une feuille métallique et des particules alpha.
Conformément au modèle atomique de Dalton, ils pensaient que les particules alpha passeraient directement à travers la feuille avec peu de déviation. Cependant, de nombreuses particules ont été déviées à des angles supérieurs à 90 °. Pour expliquer cela, Rutherford a proposé que la charge positive de l'atome soit concentrée dans un petit noyau au centre.
En 1913, le physicien Niels Bohr a proposé un modèle où les électrons orbitaient autour du noyau, mais ne pouvaient le faire que dans un ensemble fini d'orbites. Il a également proposé que les électrons puissent sauter entre les orbites, mais seulement dans des changements discrets d'énergie correspondant à l'absorption ou au rayonnement d'un photon. Cela a non seulement affiné le modèle proposé par Rutherford, mais a également donné naissance au concept d'un atome quantifié, où la matière se comportait dans des paquets discrets.

Le développement du spectromètre de masse - qui utilise un aimant pour courber la trajectoire d'un faisceau d'ions - a permis de mesurer la masse des atomes avec une précision accrue. Le chimiste Francis William Aston a utilisé cet instrument pour montrer que les isotopes avaient des masses différentes. Ceci à son tour a été suivi par le physicien James Chadwick, qui en 1932 a proposé le neutron comme un moyen d'expliquer l'existence des isotopes.
Tout au long du début du 20e siècle, la nature quantique des atomes s'est développée davantage. En 1922, les physiciens allemands Otto Stern et Walther Gerlach ont mené une expérience où un faisceau d'atomes d'argent était dirigé à travers un champ magnétique, qui était destiné à diviser le faisceau entre la direction du moment angulaire (ou spin) des atomes.
Connue sous le nom d'expérience Stern – Gerlach, les résultats ont été que le faisceau s'est divisé en deux parties, selon que le spin des atomes était orienté vers le haut ou vers le bas. En 1926, le physicien Erwin Schrodinger a utilisé l'idée de particules se comportant comme des ondes pour développer un modèle mathématique décrivant les électrons comme des formes d'onde tridimensionnelles plutôt que de simples particules.
L'utilisation de formes d'onde pour décrire les particules a pour conséquence qu'il est mathématiquement impossible d'obtenir des valeurs précises à la fois pour la position et l'impulsion d'une particule à un instant donné. Cette même année, Werner Heisenberg a formulé ce problème et l'a appelé le «principe d'incertitude». Selon Heisenberg, pour une mesure précise donnée de la position, on ne peut obtenir qu'une plage de valeurs probables pour la quantité de mouvement, et vice versa.

Dans les années 1930, les physiciens ont découvert la fission nucléaire, grâce aux expériences d'Otto Hahn, Lise Meitner et Otto Frisch. Les expériences de Hahn impliquaient de diriger des neutrons sur des atomes d'uranium dans l'espoir de créer un élément transuranium. Au lieu de cela, le processus a transformé son échantillon d'uranium-92 (Ur92) en deux nouveaux éléments - le baryum (B56) et krypton (Kr27).
Meitner et Frisch ont vérifié l'expérience et l'ont attribuée à la division des atomes d'uranium pour former deux éléments avec le même poids atomique total, un processus qui a également libéré une quantité considérable d'énergie en rompant les liaisons atomiques. Dans les années qui ont suivi, des recherches sur la possibilité d'une militarisation de ce processus ont commencé (c'est-à-dire les armes nucléaires) et ont conduit à la construction des premières bombes atomiques aux États-Unis en 1945.
Dans les années 1950, le développement d'accélérateurs de particules et de détecteurs de particules améliorés a permis aux scientifiques d'étudier les impacts des atomes se déplaçant à de hautes énergies. À partir de cela, le modèle standard de la physique des particules a été développé, qui a jusqu'à présent expliqué avec succès les propriétés du noyau, l'existence de particules subatomiques théorisées et les forces qui régissent leurs interactions.
Expériences modernes:
Depuis la seconde moitié du 20e siècle, de nombreuses découvertes nouvelles et passionnantes ont été faites en ce qui concerne la théorie atomique et la mécanique quantique. Par exemple, en 2012, la longue recherche du boson de Higgs a conduit à une percée où des chercheurs travaillant pour l'Organisation européenne pour la recherche nucléaire (CERN) en Suisse ont annoncé sa découverte.

Au cours des dernières décennies, beaucoup de temps et d'énergie ont été consacrés par les physiciens au développement d'une théorie de champ unifiée (aka. Grand Unifying Theory ou Theory of Everything). Essentiellement, depuis que le modèle standard a été proposé pour la première fois, les scientifiques ont cherché à comprendre comment les quatre forces fondamentales de l'univers (gravité, forces nucléaires fortes et faibles et électromagnétisme) fonctionnent ensemble.
Alors que la gravité peut être comprise en utilisant les théories de la relativité d'Einstein, et que les forces nucléaires et l'électromagnétisme peuvent être comprises en utilisant la théorie quantique, aucune des deux ne peut rendre compte des quatre forces travaillant ensemble. Les tentatives pour résoudre ce problème ont conduit à un certain nombre de théories proposées au fil des ans, allant de la théorie des cordes à la gravité quantique en boucle. À ce jour, aucune de ces théories n'a conduit à une percée.
Notre compréhension de l'atome a parcouru un long chemin, depuis les modèles classiques qui le voyaient comme un solide inerte qui interagissait mécaniquement avec d'autres atomes, jusqu'aux théories modernes où les atomes sont composés de particules énergétiques qui se comportent de façon imprévisible. Bien qu'il ait fallu plusieurs milliers d'années, notre connaissance de la structure fondamentale de toute matière a considérablement progressé.
Et pourtant, il reste de nombreux mystères à résoudre. Avec le temps et les efforts continus, nous pourrons enfin découvrir les derniers secrets de l'atome. Là encore, il se pourrait très bien que toute nouvelle découverte que nous fassions ne suscite que plus de questions - et pourrait être encore plus déroutante que celles qui l'ont précédée!
Nous avons écrit de nombreux articles sur l'atome pour Space Magazine. Voici un article sur le modèle atomique de John Dalton, le modèle atomique de Neils Bohr, Who Was Democritus?, Et combien d'atomes y a-t-il dans l'univers?
Si vous souhaitez plus d'informations sur l'atome, consultez l'article de la NASA sur l'analyse de petits échantillons, et voici un lien vers l'article de la NASA sur les atomes, les éléments et les isotopes.
Nous avons également enregistré un épisode entier d'Astronomy Cast consacré à l'Atom. Écoutez ici, Episode 164: Inside the Atom, Episode 263: Radioactive Decay et Episode 394: The Standard Model, Bosons.